| Темы на форуме | Автор | Дата |
В отличие от углеводородов с открытой цепью, у которых это очень затруднительно, в ароматические углеводороды легко можно ввести нитрогруппу NO2.
Для получения нитробензола нам понадобятся вначале 15 мл бензола, 20 мл концентрированной серной кислоты и 15 мл концентрированной азотной кислоты, а в конце опыта— вода и разбавленный едкий натр. Бензол очень ядовит; ни в коем случае нельзя вдыхать его пары.
Прежде всего, подготовим все необходимое оборудование. Подберем колбу Эрленмейера вместимостью 125 мл с резиновой пробкой, в отверстие которой вставлена не слишком тонкая стеклянная трубка длиной около 50 см. Нам понадобятся также делительная воронка (вместимостью 150 мл), водяная баня и термометр со шкалой до 100 °С. Подготовим еще две кастрюли — одну с ледяной водой, а другую с водой, нагретой до 60 °С.
Ввиду опасности попадания брызг в глаза, этот опыт — как и всегда при работе с концентрированными кислотами — можно проводить только в защитных очках!
В колбу Эрленмейера поместим сначала концентрированную серную кислоту и потом очень осторожно, все время слегка покачивая колбу, малыми порциями добавим азотную кислоту. Разогретую нитрующую смесь охладим, погрузив колбу в холодную воду. Затем вставим в колбу термометр и начнем постепенно добавлять бензол, непрерывно перемешивая жидкость в колбе стеклянной палочкой. Температура при этом не должна превышать 50—60 °С. Если она поднимется выше, то перед добавлением следующей порции бензола необходимо выдержать колбу в ледяной воде. Когда весь бензол будет добавлен, колбу с вертикально вставленной трубкой выдержим еще некоторое время в бане с теплой водой, температуру которой будем поддерживать от 50 до 60°С, добавляя при необходимости более горячую воду.
После этого перенесем содержимое колбы в делительную воронку. Мы обнаружим два слоя: верхний слой содержит нитробензол, а нижний — избыточную нитрующую смесь. Сольем эту смесь кислот, добавим в делительную воронку около 30 мл воды, сильно встряхнем и отделим нитробензол, который теперь, вследствие своей большой плотности, образует уже нижний слой. Для дальнейшей очистки его надо таким же образом промыть сильно разбавленным раствором едкого натра и в заключение еще раз водой.
Нитробензол — бледно-желтая жидкость с температурой кипения 210 °С и плотностью 1,203 г/см3 при 20 °С. Если во время опыта мы допустим чрезмерное повышение температуры, нитробензол будет окрашен сильнее из-за примеси динитробензола. Нитробензол очень ядовит. Нужно также остерегаться вдыхания его вредных паров с характерным сильным запахом горького миндаля. Хотя такой аромат нужен в парфюмерии, применять для этого нитробензол категорически запрещено из-за его токсичности. Обычно с той же целью используется безопасный бензальдегид, имеющий такой же запах.
 admin
admin

Нитробензол для нас — так же, как и для химической промышленности — только промежуточный продукт. Мы тоже двинемся дальше и получим из него путем восстановления анилин — родоначальник синтетических красителей.
Чтобы получить аминогруппу NHa, мы должны в нитро-группе заместить кислород водородом. В промышленности нитробензол в настоящее время восстанавливают обычно в газовой фазе, пропуская его пары в смеси с водородом над медным катализатором. Мы, работая с малыми количествами, предпочтем более старый способ, при котором восстановление осуществляется в жидкой фазе водородом в момент выделения — на латыни это называется in statu nascendi. Для этого получим водород действием соляной кислоты на железные опилки или, лучше, на гранулированный цинк или олово.
При попадании нитробензола на кожу пораженное место нужно обмыть спиртом, а затем теплой водой с мылом.
Проведем опыт следующим образом. В колбу Эрленмейера — такую же, как при получении нитробензола — поместим 10 г нитробензола и 15 г железных опилок или гранулированного цинка. Вначале добавим 5 мл концентрированной соляной кислоты и тотчас закроем колбу пробкой, в которую вертикально вставлена стеклянная трубка. При осторожном встряхивании начнется бурная реакция. При этом колба разогревается, и ее надо охладить умеренно холодной водой — так, чтобы реакция все же не остановилась совсем. Время от времени будем вынимать пробку с трубкой и добавлять еще 5—8 мл соляной кислоты.
Когда мы добавим всего 50 мл соляной кислоты, подождем, пока реакция затихнет, и в вытяжном шкафу или на открытом воздухе будем греть колбу с той же стеклянной трубкой на водяной бане от 30 минут до часа.
В заключение разбавим реакционную смесь водой и для нейтрализации кислоты добавим раствор кальцинированной или питьевой соды (бикарбоната натрия) до щелочной реакции. Для этого смесь из колбы перенесем в химический стакан и прильем сначала воду, а затем — указанный раствор. Выделится коричневая жидкость со своеобразным запахом. Это и есть анилин, который можно отделить осторожной декантацией. Лучше, хотя и хлопотнее, выделить его перегонкой с водяным паром.
Внимание! Анилин — очень сильный яд, который положено хранить только закрытым и с надписью «яд». При работе с анилином нужно остерегаться вдыхания его паров. Лучше всего — так же, как и диэтиловый эфир, — хранить анилин только в виде разбавленного спиртового раствора.
Анилин послужил исходным веществом для производства первых синтетических органических красителей. Очень давно Рунге открыл первый анилиновый краситель, который и сейчас еще используется для обнаружения анилина.
Несколько капель анилина смешаем с 10 мл воды и добавим отфильтрованный водный раствор хлорной извести. Интенсивное фиолетовое окрашивание объясняется образованием красителя, сложное строение которого явилось трудной головоломкой даже для химиков XX века. Сохраним анилин для следующих опытов и заметим в заключение, что большинство красителей в наши дни получают не из анилина, а из других соединений.
 admin
admin

Из других производных бензола упомянем здесь только фенол, толуол и нафталин. Фенол тоже был впервые обнаружен Рунге в каменноугольной смоле. Он представляет собой ароматическое соединение с гидроксильной группой и, следовательно, подобен алканолам. Однако, в отличие от алканолов, фенол имеет слабокислую реакцию и легко взаимодействует со щелочами с образованием фенолятов. Поэтому его можно растворять в щелочах. Мы уже получили родственные ему крезолы при сухой перегонке древесины и полукоксовании бурого угля. Это можно доказать, добавив к вытяжке древесного дегтя или буроугольной смолы и подсмольной воде раствор хлорида железа (III). Фенол и родственные ему вещества дают при этом окраску от синей до сине-фиолетовой. Правда, для вытяжек смолы и дегтя эта окраска может маскироваться их собственной коричневой окраской.
Чистый фенол — твердое вещество, которое плавится при 40,8 °С и кипит при 182,2 °С. При 16 °С он растворяется в 12 частях воды, причем полученный раствор окрашивает лакмусовую бумажку в красный цвет. (Проверить!) В свою очередь, фенол тоже растворяет в себе некоторое количество воды и становится жидким, даже когда в нем растворено только 5 % воды! Если мы добавим к твердому фенолу воду, то получим сначала жидкий раствор воды в феноле, а при дальнейшем добавлении воды — раствор фенола в воде.
В связи с ростом производства пластмасс фенол стал одним из важнейших промежуточных продуктов химической промышленности. Мировое производство его сейчас, по-видимому, достигает почти 200000 т в год. В Германии значительное количество фенола получается при полукоксовании бурого угля. Кроме того, все больше фенола производится путем синтеза.
 admin
admin

50 г отрубей поместим в коническую или круглодонную колбу и смешаем их со 150 мл 10—15 %-ного раствора серной кислоты. Отгоним из колбы около 100 мл жидкости. В ней содержится около 1 г растворенного фурфурола. Извлечем его из дистиллята эфиром или тетрахлорметаном и органический растворитель упарим в вытяжном шкафу. Далее проведем только две простые качественные реакции.
В первом опыте к пробе полученного раствора добавим несколько капель соляной кислоты и немного анилина. Уже на холоду возникает ярко-красная окраска.
В следующем опыте к исследуемому раствору снова добавим соляную кислоту и несколько крупинок флороглюцина (это трехатомный фенол). При кипячении появится вишнево-красная окраска.
При кипячении с разбавленными кислотами определенные типы сахаров — пентозы — образуют фурфурол. Пентозы содержатся в отрубях, соломе и т. д. и могут быть обнаружены приведенными выше методами.
 admin
admin

Нашей планете уже около 5 миллиардов лет. Вначале она, вероятно, была раскаленным газовым шаром. Позднее в результате конденсации газов возникли металлы, камень, а потом и вода. К этому времени лишь некоторые газы окружали Землю, образуя ее первоначальную атмосферу. Однако прошло несколько миллиардов лет, а планета все еще был мертва. Только около миллиарда лет назад из неживой материи появились простейшие формы жизни.
В те далекие времена в атмосфере не было чистого кислорода, но было много углекислого газа (диоксида углерода). Растения — точно так же, как и теперь — строили из него и из влаги, содержащейся в почве, сложные соединения углерода. При этом в атмосферу выделялся свободный кислород. Так постепенно образовалась современная атмосфера, содержащая много кислорода и очень мало углекислого газа.
Соединения углерода, которые накапливались в растениях ранних эпох, большей частью подверглись превращениям под влиянием анаэробных бактерий. Из остатков отмерших растений образовались торф и каменный уголь. Этому процессу способствовало высокое давление минеральных отложений, которые постепенно осаждались на остатках растений. Движение земной коры, связанное с образованием гор, также благоприятствовало появлению угля, поскольку при этом повышались давление и температура. Признаки обильного и повсеместного растительного покрова нашей планеты особенно отчетливо обнаруживаются в каменном угле той эпохи, которая началась приблизительно 400 миллионов лет назад и длилась около 55 миллионов лет. Разумеется, эти растения отличались от современных.
Судя по отпечаткам на каменном угле, в лесу тогда преобладали гигантские папоротники и плауны. По остаткам в современных образцах угля можно получить ясное представление о растительном и животном мире того времени.
Нефть и природный газ возникали на дне огромных озер и морей, где было необычайно много водорослей и водных животных. Погибая, они погружались на дно и без доступа воздуха, под влиянием бактерий превращались в гниющий ил. При гниении выделялся ядовитый сероводород, губительно действующий на остальные живые организмы. Из органических веществ возникали вначале жирные кислоты, а позднее — нефть и природный газ.— Особенно благоприятными условиями для таких процессов отличался пермский период палеозойской эры. Именно с тех пор существуют многие из крупных месторождений нефти.
На территории, где в наши дни находится ГДР, не образовалось больших запасов каменного угля и нефти. Небольшие запасы угля обнаружены в Цвиккау и Фрейтале вблизи Дрездена. Нефть и природный газ удалось найти лишь в последние годы в результате планомерного бурения скважин в Тюрингии, Бранденбурге и Меклеибургс. Управление народных предприятий нефтяной промышленности в Стендале получило задание освоить эти, хотя и не очень богатые, но все же выгодные месторождения.
 admin
admin

И сейчас в болотах гниют растения. Гниющий ил можно найти в стоячей воде пруда или вблизи от берега медленно текущего ручья. Происходящие при этом химические превращения подобны тем процессам, с которых начиналось образование угля и нефти. Проверим это с помощью опыта.
 admin
admin

Принесем из пруда немного ила. Можно взять вместо него и землю со дна болота. Вместе с илом или землей там же наберем воды. Этим илом заполним на одну треть большую стеклянную банку из-под консервов.
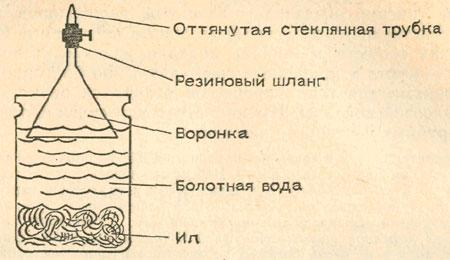
После этого доверху нальем в банку болотной воды. Сверху укрепим стеклянную воронку, а к ней куском резинового шланга присоединим короткую стеклянную трубку с оттянутым концом. Выход из воронки закроем с помощью зажима на резиновом шланге. Прибор выдержим несколько дней в достаточно теплом месте, например, около плиты или печки. Нужно только иметь в виду, что гниение сопровождается неприятным запахом.
Постепенно образуются пузырьки газа, заполняющие воронку. После этого можно с осторожностью приоткрыть зажим и тотчас поджечь выделяющийся газ. Горение обусловлено, в основном, тем, что в состав болотного газа входит метан.
Метан — первое в ряду соединение углерода. Он содержит только углерод и водород. Формула метана СН4. В его молекуле четыре атома водорода связаны с одним атомом углерода.
Однако изображенная здесь структурная формула не дает полного представления о пространственном строении молекулы метана. Исследования показали, что все четыре атома водорода находятся в вершинах правильного тетраэдра, то есть расположены одинаково относительно атома углерода, который находится в центре.
Метан получается не только при гниении. Много метана содержится в смеси газов, которая образуется при сухой перегонке угля. Кроме того, он является главной составной частью многих природных газов, а также побочным продуктом переработки нефти. В настоящее время метан служит важнейшим сырьем для получения водорода, оксида углерода СО и других веществ. При неполном сгорании метана получается сажа (углерод в тонкоизмельченном состоянии), которая используется, в частности, как наполнитель в производстве резины.
 admin
admin

Углерод, конечно, нельзя отнести к числу наиболее распространенных химических элементов. В земной коре его всего лишь 0,12 %. Но от всех остальных элементов он отличается исключительным разнообразием химических соединений. Число известных в настоящее время соединений углерода более чем вдвое превышает количество соединений всех остальных элементов, вместе взятых.
Такое своеобразие углерода объясняется особыми способностями его атомов к образованию химических связей. Как правило, углерод четырехвалентен. Его атомы могут присоединяться друг к другу с образованием более или менее длинных цепей, а также колец.
Остающиеся при этом свободные единицы валентности легко насыщаются водородом. В результате получаются углеводороды. С простейшим из них — метаном — мы уже познакомились. Следующий, более сложный углеводород называется этаном. Его молекула содержит два атома углерода и шесть атомов водорода. Присоединение третьего атома углерода и насыщение свободных валентностей водородом приводит к образованию пропана с формулой С3Н8.
Следующий углеводород с четырьмя атомами углерода называется бутаном и имеет состав С4Н10. Так же можно составить все более длинные углеродные цепи. Сейчас известны члены ряда с более чем 100 атомами углерода. Углеводороды от метана до бутана при нормальных условиях газообразны. Начиная с пентана, у которого пять атомов углерода, они представляют собой жидкости. Соединения, содержащие 17 и больше атомов углерода, при комнатной температуре являются твердыми веществами.
Углеводороды метан, этан, пропан, бутан и т. д. образуют ряд соединений, очень близких друг к другу по строению и химическим свойствам. В таблице «Ряд алканов» указаны названия и формулы важнейших членов этого ряда. Очевидно, что каждое последующее вещество отличается по составу от предыдущего наличием дополнительной группы СН2. Поэтому общая формула углеводородов с п атомами углерода СnН2n+2. Таким образом, число атомов водорода в молекуле на 2 больше, чем удвоенное число атомов углерода.
 admin
admin

В алканах все свободные валентности атомов углерода насыщены атомами водорода. Поэтому их называют еще насыщенными углеводородами. В отличие от них, ненасыщенные углеводороды содержат меньше водорода. Свободные валентности соседних атомов углерода взаимодействуют в них друг с другом и образуют двойные или тройные связи. В структурных формулах такие связи изображаются двумя или тремя черточками между соответствующими атомами углерода. Очевидно, что ненасыщенные углеводороды, если расположить их в порядке увеличения числа атомов углерода, тоже образуют гомологические ряды. Простейшие и в то же время наиболее важные в технике ненасыщенные углеводороды имеют в молекуле одну двойную или тройную связь. В первом случае они называются алкенами, а во втором — алкинами.
Первые представители этого ряда — этен (этилен) и этин (ацетилен). Этен и этин являются важнейшими промежуточными продуктами в технологии органического синтеза. Оба эти газа в настоящее время производятся во всем мире в огромных количествах путем каталитической переработки углеводородов нефти. Кроме того, большое значение имеет способ получения этина из карбида кальция и воды.
Изучение свойств ненасыщенных углеводородов начнем с этена, который легко можно получить из спирта и серной кислоты.
 admin
admin

Соберем простой прибор. Для этого понадобятся две пробирки. К одной из них подберем пробку с двумя отверстиями и вставим в нее изогнутую стеклянную трубку и термометр со шкалой до 250 °С. Все соединения должны быть достаточно плотными, чтобы образующийся газ мог выходить только через трубку.
 admin
admin







 Подготовка к ГИА и ВПР
Подготовка к ГИА и ВПР
