| Темы на форуме | Автор | Дата |
ТЕСТ по теме «Галогены»
1. Что общего в строении атомов галогенов:
а) заряд ядра атома; б) радиус атома; в) число ё на внешнем электронном слое;
г) до октета (восьми e-) на внешнем электронном слое недостает по одному e-?
2. В чем различие строения атомов галогенов:
а) заряд ядра атома; б) радиус атома; в) внешний электронный слой близок к завершенному;
г) относительная атомная масса?
3. Особенности в строении атомов галогенов, обусловливающие их принадлежность к типичным неметаллам:
а) заряд ядра атома; б) радиус атома; в) общее число e-; г) близкое к завершению общее число e-, находящихся на внешнем электронном слое, и способность атома легко принимать недостающие для этого электроны.
4. Как изменяются неметаллические свойства галогенов в группе с увеличением порядкового номера:
а) возрастают; б) не изменяются; в) уменьшаются; г) усиливаются от элемента № 17 к элементу № 9, остальные - без изменения?
5. Галогены являются:
а) сильными восстановителями; б) сильными окислителями; в) переходными элементами?
6. Установите соответствие, характеризуя физические свойства галогенов:
1) фтор А. красно-бурая жидкость
2) хлор Б. светло-желтый газ
3) бром В. твердое кристаллическое вещество, темно-фиолетовое, с металлическим блеском
4) йод Г. газ, желто-зеленый
*7. Галогены - простые вещества — имеют одинаковый вид химической связи в молекуле, но разное агрегатное состояние. Это объясняется тем, что:
а) галогены образуют кристаллы разной формы; б) в узлах кристаллической решетки находятся двухатомные молекулы с разной массой и силой притяжения; в) окислительная активность галогенов неодинакова.
8. Назовите жидкий галоген: а) хлор; б) фтор; в) бром; г) йод.
*9. Назовите галоген, который способен возгоняться: а) фтор; б) хлор; в) бром; г) йод.
10. Какое из приведенных ниже утверждений является неверным? Галогены обладают следующими свойствами:
а) в газообразном состоянии существуют в виде двухатомных молекул;
б) способны образовывать со щелочными металлами соединение типа MeR;
в) не образуют химической связи с Н2;
г) обладают окислительными свойствами.
11. Составьте из следующих словосочетаний два правильных суждения о галогенах:
а) с возрастанием заряда ядра в подгруппе галогенов; д) окислительные свойства галогенов;
б) с уменьшением заряда ядра в подгруппе галогенов; е) усиливаются;
в) от фтора до астата; ж) ослабевают. г) от астата до фтора;
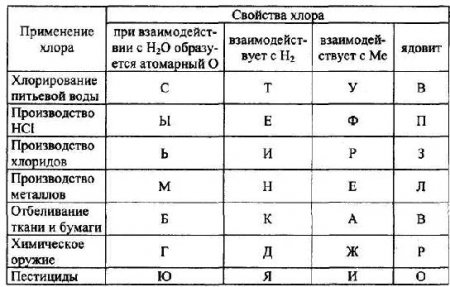
12. Найдите области применения хлора в зависимости от его свойств.
Из букв, соответствующих правильным ответам, получите название металла, ионы которого служат реактивом на хлорид-ионы.
13. Какая из приведенных реакций протекает в растворе? a) KI + Вг2 ; б) КВг +I2 →; в) КС1 + Вг2 ; г) КС1 +I2
14. Какой атом наиболее сильный окислитель: a) ...2s22p5; б) ...3s23p5; в) ...3d'°4s24p5; г) ...4dI05s25p5?
15. Какая схема отражает лабораторный способ получения хлороводорода?
а) Н2 + С12 →; б) NaCl + H2SO4 →; в) СН, + Cl2 →
16. В каком случае реакция пройдет до конца? a) Na+ + СI- →; б) Са2+ + СI- → в) Ag+ + СI- → г) А13+ + СI- →
17. Какая из реакций, используемых в превращении:
А Б В
НС1 —> С12 —> НС1 → AgCl, является реакцией обмена?
18. Соляную кислоту и хлориды можно распознать по их реакции:
а) с нитратом серебра; б) с серебром; в) с хлоридом серебра.
19. Соляная кислота обладает свойствами: 1) изменять окраску лакмуса; 2) изменять цвет фенолфталеина; 3) реагировать со многими металлами; 4) растворять медь; 5) нейтрализовать гидроксид кальция; 6) растворять оксид золота; 7) взаимодействовать с солями; 8) вытеснять серную кислоту из сульфатов.
20. На схеме изображены области применения галогенов и их соединений. Найдите соответствие:
а) хлор; б) бром; в) фтор; г) йод.
|
|
травление стекла |
|
бумажная промышленность |
|
получение высокочистых Me |
органический синтез |
органический синтез |
органический синтез |
|
лекарственные препараты для щитовидной железы |
охлаждающие вещества |
фотоэмульсия |
металлургия |
|
органический синтез |
жидкое топливо для ракет |
лекарства |
лекарства |
|
производство антисептиков |
пластмассы и красители |
красители |
пластмассы и красители |
1 2 3 4
ТЕСТ 1. ГАЛОГЕНЫ. Вариант 1
1. В ряду элементов VII А группы Периодической системы Д.И. Менделеева F-CI-Br-J:
а) металлические свойства усиливаются б) неметаллические свойства усиливаются
в) неметаллические свойства ослабевают
г) неметаллические свойства сначала растут, затем уменьшаются
2. Укажите сходство в строении атомов галогенов.
а) заряд ядра атома б) радиус атома
в) одинаковое число электронов на внешнем энергетическом уровне
г) до завершения внешнего уровня (до октета) недостает по одному электрону
3. Отметьте характеристики галогенов.
а) молекулы двухатомны в газообразном состоянии m б) ЭО(F) > ЭО(СI) > ЭО(Вг) > Э0(J)
в) проявляют степень окисления от -1 до +7 (исключение F-1)
г) обладают только окислительными свойствами
4. Плотность, температуры плавления и кипения галогенов с увеличением заряда ядра атома в подгруппе Периодической системы Д.И. Менделеева:
а) уменьшаются б) возрастают в) не изменяются г) уменьшаются, затем возрастают
5. Наиболее сильно окислительные свойства выражены у:
а) фтора б) хлора в) брома г) йода
6. Восстановительные свойства наиболее сильно выражены у:
а) фтора б) хлора в) йода г) брома
7. Наиболее сильная энергия ионизации выражена у:
а) фтора б) хлора в) брома г) йода
8. Сила галогеноводородных кислот возрастает в ряду:
а) HI, HBr, HCI б) HCI, HBr, HJ в) HBr, HJ, HCI г) HJ, HCI, HBr
9. Водные растворы практически не образуют: а) фтор б) хлор в) бром г) йод
10. Вид химической связи и тип кристаллической решетки в соединениях галогенов с
металлами соответственно:
а) ковалентная полярная; молекулярная в) ионная; ионная
б) металлическая; металлическая г) ковалентная неполярная; молекулярная
11. Определите, какая из приведенных реакций протекает в растворе.
а) KBr + J2 ® б) КСI + Вг2 ® в) КСI + J2 ® г) KBr + СI2 ®
ТЕСТ 1 ГАЛОГЕНЫ. Вариант 2
1. В ряду элементов VII А группы Периодической системы Д.И. Менделеева F-CI-Br-J:
а) окислительные свойства усиливаются
б) окислительные свойства ослабевают
в) восстановительные свойства усиливаются
г) восстановительные свойства ослабевают
2. Укажите различия в строении атомов галогенов.
а) заряд ядра атома
б) радиус атома
в) внешний энергетический уровень близок к завершению
г) в основном состоянии один неспаренный p-электрон на внешнем энергетическом уровне
3. Отметьте характеристики галогенов.
а) в ряду F2— CI2 — Вг2 — J2 изменяется масса молекул, находящихся в узлах кристаллической решетки, и сила притяжения между молекулами
б) валентность в соединениях переменная, от I до VII, степень окисления от -1 до +7 (искл. фтор -1)
в) Э0(J) > ЭО(Вг) > ЭО(СI) > ЭО(F) г) не реагируют с кислородом и азотом
4. Агрегатное состояние и окраска галогенов простых веществ постепенно изменяются с
увеличением порядкового номера химического элемента в Периодической системе.
Выберите ответ, в котором охарактеризованы эти свойства брома.
а) газ, зелено-желтый в) твердое кристаллическое вещество, черное с серым отливом
б) газ, желто-зеленый г) жидкость, красно-бурая
5. Самым сильным окислителем является: а) бром б) хлор в) фтор г) йод.
6. Наиболее сильно восстановительные свойства выражены у:
а) фтора б) хлора в) брома г) йода
7. Наиболее сильное сродство к электрону выражено у:
а) фтора б) хлора в) брома г) йода
8. Агрегатное состояние и окраска галогенов простых веществ постепенно изменяются с увеличением порядкового номера химического элемента в Периодической системе Д.И. Менделеева. Выберите ответ, в котором даны характеристики этих физических свойств йода.
а) газ, зелено-желтый б) газ, желто-зеленый
в) твердое кристаллическое вещество, черное с серым отливом
г) жидкость, красно-бурая
9. Вид химической связи и тип кристаллической решетки в молекулах галогенов
соответственно:
а) ковалентная полярная; молекулярная в) ковалентная неполярная; молекулярная
б) металлическая; металлическая г) ионная; ионная
10. Прочность химической связи в ряду HF-HCI-HBr-HI:
а) возрастает б) падает в) не изменяется г) сначала падает, затем возрастает
11. Определите, какая из приведенных реакций протекает в растворе.
а) KI + Вг2 ® б) КВг2 + J2 ® в) КСI + Вг2 ® г) КСI + J2 ®
Своё Спасибо, еще не выражали..
 admin
admin







 Подготовка к ГИА и ВПР
Подготовка к ГИА и ВПР
