| Темы на форуме | Автор | Дата |
Сначала сплавим свинец с оловом и получим сплав, примерно соответствующий составу припоя.
Поместим в тигель несколько граммов свинца и расплавим его. Затем добавим олово и хорошо перемешаем расплав железной проволокой. Возьмем тигель щипцами и поставим его в цветочный горшок, на одну треть наполненный сухим песком. Термометр, опущенный в тигель, покажет температуру 300—360 °С. Во время охлаждения каждые полминуты будем отмечать температуру и заносить ее в подготовленную заранее таблицу, где в левом столбце отмечается время, а в правом — температура. После полного затвердевания еще несколько минут проследим за ходом охлаждения и затем прекратим опыт.
Тот, кто хочет получить полное представление о термическом поведении сплава, должен начать опыты с чистого свинца и затем перейти к добавлению сначала небольших, а затем все увеличивающихся, точно взвешенных количеств олова. Таким образом можно снова использовать предыдущие сплавы.
Найденную взаимосвязь представим графически. На листе миллиметровой бумаги отложим на оси абсцисс (горизонтально) время, а на оси ординат (вертикально) — температуру.
 admin
admin

Самое большое значение среди всех сплавов имеют стали различных составов. Простые конструкционные стали состоят из железа относительно высокой чистоты с небольшими (0,07—0,5 %) добавками углерода, а легированные стали получают, добавляя к железу кремний, медь, марганец, никель, хром, вольфрам, ванадий и молибден.
Мы удовлетворимся некоторыми простыми опытами. Для экспериментов по закалке возьмем отслужившие лезвия безопасной бритвы. Применим не только простые стальные лезвия, но и лезвия из нержавеющей легированной стали, такие как «Polsilver» или «Chroma».
Лезвия изготовлены из очень мягкого материала, ими нельзя, например, поцарапать стекло. Если взять лезвие пинцетом или щипцами и подержать в несветящемся пламени бунзеновской горелки, то поверхность его станет сначала желтой, затем голубой и наконец серой. Это в результате нагревания появились цвета побежалости в тонких пленках железной окалины Fe3О4. Если светло-красное раскаленное лезвие быстро погрузить в холодную воду, то слой, образовавшийся в окислительной атмосфере, отделится в виде блесток.
Сталь станет хрупкой и легко сломается при сгибании. Но зато повысится ее твердость, так что можно будет без труда поцарапать стекло. Чтобы избавиться от хрупкости, сохранив большую твердость, после быстрого охлаждения сталь «отпускают», короткое время нагревая ее при температуре 220—700 °С в зависимости от качества и целей применения.
Если на закрытой плитке или на масляной бане (Осторожно!) нагреть лезвия до 230—330 °С, мы опять увидим сначала желтый, затем коричневый, красный, голубой и, наконец, серый цвета побежалости.
Часто граммофонные иглы и лезвия безопасных бритв обрабатывают «отпуском» до желтого цвета при 230 °С, часовые стрелки — до светло-голубого при 310 °С, пилы и ножи — до василькового при 295 °С.
Исключительные механические свойства при отличной коррозионной стойкости имеют высоколегированные, и потому дорогие, хромоникелевые стали. Самую распространенную из них мы уже упоминали как сталь 18/8. Входящий в ее состав хром, образуя пассивирующую поверхностную пленку (подробнее см. в разделе «Небольшой курс электрохимии металлов»), сильно повышает коррозионную стойкость, а добавка никеля улучшает механические свойства.
В нескольких опытах убедимся прежде всего в том, что пробы из нержавеющей стали (нержавеющие лезвия, сломанные ножи) почти не разрушаются сильной азотной или серной кислотой. Однако соляная кислота, вследствие частичного разрушения защитного слоя, подвергает сталь сквозной коррозии. Чтобы перевести в раствор небольшое количество металла, обработаем в пробирке стальную пробу царской водкой. (Царская водка состоит из 3 объемных частей концентрированной соляной и 1 части концентрированной азотной кислоты. Внимание! Смесь очень агрессивна, пары ядовиты!). Затем осторожно разбавим раствор водой примерно в пятикратном размере, нейтрализуем, постепенно добавляя раствор соды, и проведем описанные выше реакции обнаружения хрома, никеля и молибдена. Часто нержавеющие стали содержат около 2 % молибдена — это дополнительно увеличивает твердость изготовленных из них инструментов.
Мы предоставляем самому читателю подвергнуть коррозионным испытаниям железные или стальные пробы различного происхождения и обработки. Для этой цели частично погрузим их в водные растворы, которые находятся на дне стеклянных сосудов (например, стеклянных банок). Рекомендуем проверить действие обычной и дистиллированной воды, соленой воды, растворов хлорида магния, аммиака, сернистой кислоты, а также разбавленных минеральных и органических кислот. В малоагрессивных жидкостях ржавчина интенсивнее всего образуется вблизи поверхности раствора, потому что здесь самое высокое содержание кислорода. Сильное коррозионное воздействие оксида серы (IV) является важнейшей проблемой при очистке промышленных отработанных газов, которые выделяются в процессе переработки угля и руд и содержат SO2.
 admin
admin

 admin
admin

Основополагающим звеном для понимания электрохимических процессов является ряд напряжения металлов. Металлы можно расположить в ряд, который начинается с химически активных и заканчивается наименее активными благородными металлами:
Li, Rb, К, Ва, Sr, Ca, Mg, Al, Be, Mn, Zn, Cr, Ga, Fe, Cd, Tl, Co, Ni, Sn, Pb, H, Sb, Bi, As, Cu, Hg, Ag, Pd, Pt, Au.
Так выглядит, по новейшим представлениям, ряд напряжений для важнейших металлов и водорода. Если из двух любых металлов ряда изготовить электроды гальванического элемента, то на предшествующем в ряду материале появится отрицательное напряжение. Величина напряжения (разность потенциалов) зависит от положения элемента в ряду напряжений и от свойств электролита.
Сущность ряда напряжения установим из нескольких простых опытов, для которых нам понадобятся источник тока и электрические измерительные приборы.
 admin
admin

Металлические покрытия, «деревья» и «ледяные узоры» без тока → Химия / Практическая химия / Металлы - основа техники
Растворим около 10 г кристаллического сульфата меди в 100 мл воды и погрузим в раствор стальную иглу или кусочек железной жести. (Рекомендуем предварительно до блеска зачистить железо тонкой наждачной шкуркой.) Через короткое время железо покроется красноватым слоем выделившейся меди. Более активное железо вытесняет медь из раствора, причем железо растворяется в виде ионов, а медь выделяется в виде металла. Процесс продолжается до тех пор, пока раствор находится в контакте с железом. Как только медь покроет всю поверхность железа, он практически прекратится. В этом случае образуется довольно пористый слой меди, так что защитные покрытия без применения тока получать нельзя.
В следующих опытах опустим в раствор сульфата меди небольшие полоски цинковой и свинцовой жести. Через 15 минут вытащим их, промоем и исследуем под микроскопом. Мы различим красивые, похожие на ледяные, узоры, которые в отраженном свете имеют красную окраску и состоят из выделившейся меди. Здесь также более активные металлы перевели медь из ионного в металлическое состояние.
В свою очередь, медь может вытеснять металлы, стоящие ниже в ряду напряжений, то есть менее активные. На тонкую полоску листовой меди или на расплющенную медную проволоку (предварительно зачистив поверхность до блеска) нанесем несколько капель раствора нитрата серебра. Невооруженным взглядом можно будет заметить образовавшийся черноватый налет, который под микроскопом в отраженном свете имеет вид тонких игл и растительных узоров (так называемых дендритов).
Чтобы выделить цинк без тока, необходимо применить более активный металл. Исключая металлы, которые бурно взаимодействуют с водой, находим в ряду напряжений выше цинка магний. Несколько капель раствора сульфата цинка поместим на кусок магниевой ленты или на тонкую стружку электрона. Раствор сульфата цинка получим, растворив кусочек цинка в разбавленной серной кислоте.
Одновременно с сульфатом цинка добавим несколько капель денатурата. На магнии через короткий промежуток времени заметим, особенно под микроскопом, выделившийся в виде топких кристалликов цинк.
В общем, любой член ряда напряжения может быть вытеснен из раствора, где он находится в виде иона, и переведен в металлическое состояние. Однако при испытании всевозможных комбинаций, нас может постичь разочарование. Казалось бы, если полоску алюминия погрузить в растворы солей меди, железа, свинца и цинка, на ней должны выделяться эти металлы. Но этого, однако, не происходит.
Причина неудачи кроется не в ошибке в ряду напряжений, а основана на особом торможении реакции, которое в данном случае обусловлено топкой оксидной пленкой на поверхности алюминия. В таких растворах алюминий называют пассивным.
 admin
admin

Чтобы сформулировать закономерности протекающих процессов, мы можем ограничиться рассмотрением катионов, а анионы исключить, так как они сами в реакции не участвуют. (Правда, на скорость осаждения влияет вид анионов.) Если для простоты предположить, что и выделяющийся и растворенный металлы двухвалентные, то можно записать:

причем для первого опыта Me1 = Fe, Me2 = Сu. Итак, процесс состоит в обмене зарядами (электронами) между атомами и ионами обоих металлов. Если отдельно рассматривать (в качестве промежуточных реакций) растворение железа или осаждение меди, то получим:
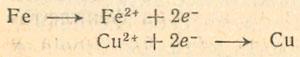
Теперь рассмотрим случай, когда металл погружен в воду или в раствор соли, с катионом которой обмен невозможен из-за его положения в ряду напряжений. Несмотря на это, металл стремится перейти в раствор в виде иона. При этом атом металла отдает два электрона (если металл двухвалентный), поверхность погруженного в раствор металла заряжается по отношению к раствору отрицательно, а на границе раздела образуется двойной электрический слой. Эта разность потенциалов препятствует дальнейшему растворению металла, так что процесс вскоре приостанавливается. Если в раствор погрузить два различных металла, то они оба зарядятся, но менее активный — несколько слабее, в силу того, что его атомы менее склонны к отщеплению электронов. Соединим оба металла проводником. Вследствие разности потенциалов поток электронов потечет от более активного металла к менее активному, который образует положительный полюс элемента. Протекает процесс, при котором более активный металл переходит в раствор, а катионы из раствора выделяются на более благородном металле.
 admin
admin

Проиллюстрируем теперь несколькими опытами приведенные выше несколько абстрактные рассуждения (которые к тому же представляют собой грубое упрощение).
Сначала наполним химический стакан вместимостью 250 мл до середины 10 %-ным раствором серной кислоты и погрузим в нее не слишком маленькие куски цинка и меди. К обоим электродам припаяем или приклепаем медную проволоку, концы которой не должны касаться раствора.
Пока концы проволоки не соединены друг с другом, мы будем наблюдать растворение цинка, которое сопровождается выделением водорода. Цинк, как следует из ряда напряжения, активнее водорода, поэтому металл может вытеснять водород из ионного состояния. На обоих металлах образуется двойной электрический слой. Разность потенциалов между электродами проще всего обнаружить с помощью вольтметра. Непосредственно после включения прибора в цепь стрелка укажет примерно 1 В, по затем напряжение быстро упадет. Если подсоединить к элементу маленькую лампочку, потребляющую напряжение 1 В, то она загорится — сначала довольно сильно, а затем накал станет слабым.
По полярности клемм прибора можно сделать вывод, что медный электрод является положительным полюсом. Это можно доказать и без прибора, рассмотрев электрохимию процесса. Приготовим в маленьком химическом стакане или в пробирке насыщенный раствор поваренной соли, добавим примерно 0,5 мл спиртового раствора индикатора фенолфталеина и погрузим оба замкнутых проволокой электрода в раствор. Около отрицательного полюса будет наблюдаться слабое красноватое окрашивание, которое вызвано образованием на катоде гидроксида натрия.
В других опытах можно помещать в ячейку различные пары металлов и определять возникающее напряжение. Например, магний и серебро дадут особенно большую разность потенциалов благодаря значительному расстоянию между ними в ряду напряжений, а цинк и железо, наоборот, очень маленькую, менее десятой доли вольта. Применяя алюминий, мы не получим из-за пассивации практически никакого тока.
Все эти элементы, или, как говорят электрохимики, цепи, имеют тот недостаток, что при съеме тока на них очень быстро падает напряжение. Поэтому электрохимики всегда измеряют истинную величину напряжения в обесточенном состоянии с помощью метода компенсации напряжения, то есть сравнивая его с напряжением другого источника тока.
Рассмотрим процессы в медно-цинковом элементе несколько подробнее. На катоде цинк переходит в раствор по следующему уравнению:
 admin
admin

 admin
admin

Почти все важнейшие части орудий производства, начиная простейших механизмов и кончая сложными машинами, изготовлены из металлов. Хотя широко используемые в последнее время пластмассы частично заменяют металлы, производство металлов все время возрастает, и в будущем все равно главным образом из них будут изготовлять большинство промышленных установок, машины, моторы, электрическую проводку, котлы высокого давления и т. д.
Перечислим некоторые характерные свойства металлов: металлы можно отливать, ковать, вальцевать, вытягивать в проволоку, гнуть, сваривать, паять, обтачивать, сверлить, пилить, строгать.
Сплавляя металлы или вводя в них небольшие добавки неметаллов, можно получать материалы, отвечающие специальным требованиям.
Инструменты для обработки металлов (токарные резцы, сверла, специальные пилы и т. д.) должны обладать повышенной твердостью, а листовые или винтовые рессоры, напротив, отличаться эластичностью и одновременно прочностью. От зубчатых колес, валов, болтов и гаек требуется особенная прочность на излом, от тросов и цепей — чрезвычайное сопротивление растяжению, а колбам, цилиндрам, котлам высокого давления приходится переносить высокую температуру, огромное давление и воздействие химически агрессивных веществ.
Без металлов не было бы электротехники. Хорошая проводимость электрического тока характерна для всех «настоящих металлов» и не присуща неметаллическим материалам. Из более чем 90 химических элементов, встречающихся в природе, около 65 причисляют к металлам. Некоторые элементы, такие как сурьма или полупроводник германий, стоят на границе между металлами и неметаллами.
Еще 200 лет назад большая часть этих металлов не имела никакого технического значения. Довольствовались обычными, в основном легко получаемыми, металлами. Только с наступлением атомного века, при постройке сверхзвуковых самолетов и космических ракет, требования к металлическим материалам резко повысились. Уже в начале прошлого века потребности авиационной промышленности привели к развитию производства легких металлов: алюминия и магния. Многочисленные изобретения сделали возможным создание установок для получения таких металлов, названия которых сравнительно недавно были известны немногим. Это прежде всего титан и цирконий, которые встречаются часто, но в основном рассеяны в горных породах и редко встречаются в виде чистых руд. Техническое значение приобрели также бериллий, гафний, индий, ниобий и другие экзотические металлы.
Уран и плутоний служат сегодня горючим для ядерных реакторов, в которых получают тонны трансуранового элемента плутония.
Плутоний можно назвать искусственным элементом — в природе он практически не встречается. В результате ядерного расщепления 1 кг плутония выделяется примерно столько же энергии, как при сгорании 2500т каменного угля или при взрыве такого же количества тринитротолуола!
 admin
admin

По экспериментальной химии металлов и их соединений можно было бы написать объемистую книгу. До сих пор, изучая с помощью несложных опытов некоторые свойства металлов и их солей, мы в лучшем случае могли сделать многосторонний, но несистематический и далеко не полный обзор. Теперь уделим особенное внимание распределению металлов по группам и важнейшим свойствам этих групп. Далее мы рассмотрим реакции, по которым можно установить наличие определенного металла в смеси веществ.
Для этих опытов нам понадобятся образцы чистых металлов или их сплавов, которые можно изготовить из старых металлических предметов. Токарная стружка и металлические опилки, остатки медной проволоки, старые никелевые и серебряные монеты, алюминиевая фольга и испорченные хромированные части велосипеда, цинковая пластинка из использованной батарейки для карманного фонарика, кусок старого водосточного желоба, свинец из аккумуляторной пластины или из остатка кабеля, оловянная фольга или оловянные фигурки, вольфрамовая пить накаливания из перегоревшей лампочки, молибденовый держатель нити накаливания или сетка использованной радиолампы, никелевый анод этой же лампы — вот некоторые, далеко не полные возможности для заготовки металлических образцов. Само собой разумеется нам потребуются очень небольшие количества дорогих цветных металлов, которые надо постараться извлечь из металлолома.
Наряду с этими образцами воспользуемся также соединениями металлов, которые можно приобрести, так же как и другие химикаты, в аптеке, хозяйственном магазине, в специализированном магазине реактивов и т. д.
В химии металлы классифицируют по их положению в периодической системе элементов. Практики, кроме того, подразделяют металлы на тяжелые и легкие, благородные и неблагородные, тугоплавкие и легкоплавкие, а также классифицируют их с других точек зрения.
Периодическая система состоит, как известно, из групп, которые в свою очередь включают в себя главные и побочные подгруппы элементов, обладающих схожими химическими свойствами, в таблице они расположены друг под другом. В главной подгруппе первой группы находятся щелочные металлы — литий, калий, натрий, рубидий и цезий, а в побочной подгруппе первой группы — медь, серебро и золото. В главную подгруппу второй группы включены щелочноземельные металлы бериллий, магний, кальций, стронций, барий, радий, а в побочную — цинк, кадмий и ртуть. Третья группа начинается с неметалла бора, затем идут металлы, образующие «земли»: алюминий, скандий, иттрий, 15 редкоземельных элементов и радиоактивный актиний. В соответствующей побочной подгруппе находятся мало известные металлы галлий, индий и таллий. В главных подгруппах четвертой и пятой групп металлический характер обнаруживают только последние члены группы, а в главных подгруппах шестой, седьмой и восьмой групп находятся только неметаллы. Но элементы побочных подгрупп этих групп периодической системы являются металлами. Особенно важны так называемые переходные металлы побочной подгруппы восьмой группы, которые образуют три подгруппы. Здесь содержатся металлы подгруппы железа и платины. Разделение на группы можно объяснить с помощью атомной теории, но здесь это было бы излишним.
 admin
admin







 Подготовка к ГИА и ВПР
Подготовка к ГИА и ВПР
