| Темы на форуме | Автор | Дата |
Открытый в 1863 г. Анилиновый черный относится к числу старейших органических красителей. Это популярный краситель хиноидного строения, имеющий брутто-формулу C48H34N8.
В пробирке к 0,5 мл анилина прильем равный объем концентрированной соляной кислоты, смесь взболтаем и медленно добавим 7 мл воды. Затем прильем к смеси еще 4 мл концентрированного раствора бихромата калия и оставим реакционную массу на 5—10 минут. При этом появится черная окраска. Выльем раствор в химический стакан на 100 мл, нагреем его до кипения и будем кипятить 0,5—1 минуту, а потом охладим. Образовавшийся Анилиновый черный отфильтруем, краситель на фильтре промоем водой. Он не растворяется в воде и спирте. Темный фильтрат можно вылить.
Столь давно найденный Лайтфутом Анилиновый черный замечателен своим великолепным, «сочным» черным цветом, на фоне которого особенно ярко выглядят рисунки, нанесенные другими красителями. В этом отношении с ним и сейчас не может сравниться ни один из черных красителей других классов. Поэтому вопрос о его строении в течение многих лет привлекает к себе внимание химиков. Однако загадка оказалась весьма сложной и до сих пор не решена до конца. Существенный вклад в решение вопроса внесли Внльштеттер и Грин (через 50 лет после открытия красителя!), а также советский химик И. С. Иоффе.
 admin
admin

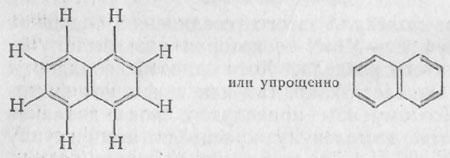
Рассматривая структурную формулу нафталина, мы видим, что она состоит из двух колец, имеющих два общих атома углерода. Поэтому нафталин относится к числу конденсированных циклических соединений.
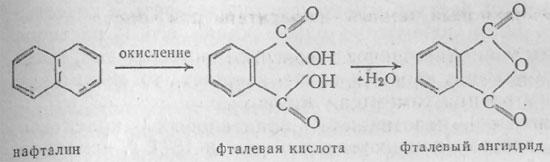
Из нафталина путем каталитического окисления получается фталевая (1,2-бензолдикарбоновая) кислота, а из нее при отщеплении воды — соответствующий ангидрид.
 admin
admin

Фталевая кислота продается в магазинах химических реактивов. Для наших опытов мы сами получим фталевый ангидрид:
На песочной бане медленно нагреем в фарфоровой чашке небольшое количество фталевой кислоты. Чашку накроем часовым стеклом такого же диаметра. Фталевая кислота плавится при 230 °С. На стекле мы вскоре увидим красивые длинные иглы возгоняющегося фталевого ангидрида. Из него мы получим три любопытных красителя.
 admin
admin

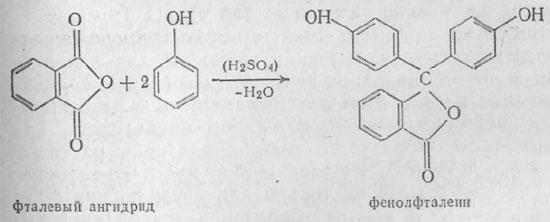
В фарфоровой чашке тщательно перемешаем несколько кристаллов гидроксибензола (фенола) с трехкратным количеством фталевого ангидрида. Пипеткой будем добавлять по каплям серную кислоту — до тех пор, пока смесь полностью не пропитается жидкостью. Теперь при непрерывном перемешивании стеклянной палочкой подвергнем содержимое чашки на малом пламени горелки через асбестированную сетку нагреванию в течение нескольких минут. Когда появится белый дым, ненадолго прекратим нагревание, иначе потеряется слишком много фталевого ангидрида, который кипит при 131,6 °С. В конце опыта мы увидим, что плав приобретает окраску — от коричнево-красной до оранжевой. Реакция окончена:
 admin
admin

Препараты для подцвечивания и отдушивания воды в ванне наряду с различными солями и эфирными маслами содержат краситель, который поглощает падающий свет и тотчас излучает его обратно. Излучаемый свет обладает меньшей энергией и, следовательно, характеризуется большими длинами волн, чем поглощенный. Это явление называется флуоресценцией, а краситель — флуоресцеином.
Проведем опыт точно так же, как и получение фенолфталеина, только вместо гидроксибензола (фенола) возьмем один из его аналогов—1,3-дигидроксибензол (резорцин) в количестве, равном количеству фталевого ангидрида. Реакционную массу постепенно нагреем до 180 град. С.
Плав получается густым и имеет кроваво-красную окраску. Дадим ему застыть и половину сохраним для дальнейших опытов, а другую половину переработаем следующим образом. Поместим плав в пробирку, перемешаем с разбавленным водным раствором аммиака или едкого натра, слегка нагреем и взболтаем. Образуется соль, придающая раствору интенсивное окрашивание. Щелочи нужно взять достаточно, поскольку она необходима не только для превращения флуоресцеина в соль, но и для нейтрализации серной кислоты. (Осторожно! При нейтрализации выделяется тепло.)
Одну каплю раствора добавим в большую пробирку с водой и перемешаем. Если теперь посмотреть на раствор против света, то он выглядит желтым. Если же смотреть на него в отраженном свете — сверху или но направлению падающего света на темном фоне, то заметна зеленая флуоресценция.
Благодаря флуоресценции можно обнаружить этот краситель в самой малой концентрации. Флуоресценция хорошо заметна даже при растворении 1 г вещества в 40000 л воды! 250 г этого красителя достаточно для подцвечивания воды в бассейне для плавания длиной 100 м, шириной 25 м и глубиной 2 м. Способность флуоресцсина необычайно легко обнаруживаться в ничтожно малых концентрациях используют для определения направления подземных водных течений.
Примером может сложить решение вопроса об «исчезновении» Дуная. В верховье этой реки, вблизи железнодорожной станции Иммединген, большая часть дунайской воды теряется в рыхлых известняковых породах. Чтобы установить направление движения воды в 1877 г, вблизи этой станции в Дунай высыпали 10 кг флуоресцеина. Через 60 часов один из выставленных постов обнаружил в маленькой речушке Аах в Хегау отчетливую флуоресценцию. Тем самым, было доказано, что вода Дуная большей частью просачивается в испещренный трещинами известняк, достигает удаленной за 15 км речки Аах и оттуда выходит в подземное озеро, примыкающее к Боденскому озеру.
 admin
admin

Близкий родственник флуоресцеина — краситель, получивший свое название от греческого слова «эос» (утренняя заря). Он образует темно-красные кристаллы, которых растворяются в воде с образованием яркой розовой окраски. Как только эозин был открыт, он сразу же стал одним из самых любимых красителей для тканей из шерсти, хлопка и шелка.
Эозин мы найдем и в губной помаде, и в составе краски для знаков опасности; кондитеры применяют его для окраски сладостей, биологи — для окрашивания микробов.
Для получения эозина нужно иметь несколько капель брома, поэтому опыт можно проводить только в химическом кружке. Бром — сильный яд! Пары его раздражают глаза и дыхательные пути, а брызги вызывают на коже болезненные ожоги. Поэтому опыты с бромом можно проводить только в резиновых перчатках и защитных очках в вытяжном шкафу или на открытом воздухе.
К остатку полученного нами ранее флуоресцеина в фарфоровой чашке добавим 1—2 капли брома и слегка нагреем. После охлаждения добавим несколько миллилитров раствора едкого натра. Когда появится красное окрашивание, одну каплю раствора красителя разбавим водой, чтобы можно было наблюдать флуоресценцию. Остальную часть красителя используем для цветных реакций.
Например, при анализе органических соединений для обнаружения брома в присутствии хлора можно воспользоваться эозиновой пробой.
Приготовим флуоресцеиновую бумагу. Для этого пропитаем фильтровальную бумагу раствором флуоресцеина, высушим ее и разрежем на полоски величиной с полоски лакмусовой бумаги. На такую полоску нанесем малое количество исследуемого вещества и выдержим ее над отверстием бутылки с концентрированным водным раствором аммиака. В присутствии брома бумага на обработанном месте приобретает бледно-розовую окраску.
В заключение еще раз сравним формулы всех трех родственных красителей. Мы видим, что все они имеют общую основу — трифенилметан.
 admin
admin

Современные лекарства все больше способствуют сохранению нашего здоровья и продлению жизни. Многие вызывавшие ранее ужас инфекционные заболевания теперь не так страшны благодаря наличию антибиотиков. Помимо них, в распоряжении врачей сегодня имеются тысячи других препаратов для лечения и для предотвращения заболеваний. В области фармацевтической химии и фармацевтической промышленности успешно осуществляется кооперация между странами социалистического содружества. Возникает взаимовыгодное разделение труда, и специализация каждой страны на определенных видах лекарств позволяет добиться большей эффективности производства.
В самом деле, среди лекарств, которые выписывает нам врач, мы нередко обнаруживаем препараты, выпущенные в Польше, Чехословакии или Венгрии. Разумеется, фармацевтические предприятия в Германии тоже вносят существенный вклад в изготовление новых ценных лекарственных средств, все шире обеспечивая ими социалистические страны и многие другие государства, в том числе развивающиеся страны Африки и Латинской Америки.
Крупнейший в Германии завод лекарственных препаратов «Иенафарм» в г. Иена вырос на базе маленькой лаборатории предприятия «Ненауэр Гласверке Шотт». В свое время эта лаборатория получила задание как можно быстрее удовлетворить неотложную потребность в пенициллине и других важных лекарственных препаратах и в кратчайший срок добилась значительных успехов, что привело к ее расширению. Теперь завод «Иена-фарм» располагает обширными и светлыми, удобными для работы новыми зданиями и выпускает почти 25 % всей продукции химико-фармацевтической промышленности Германии. Здесь трудятся для сохранения нашего здоровья 2500 человек, из них больше половины — женщины. Они выпускают продукцию только отличного качества.
Педантичнейшая аккуратность, соблюдение порядка и чистоты, тщательная проверка качества выпускаемых препаратов являются на таких предприятиях нерушимыми заповедями. В важнейших цехах, где изготавливают антибактериальные вакцины и сыворотки, должно быть полностью исключено проникновение в воздух болезнетворных микробов. Поэтому сюда можно войти только через бокс, в котором посетителя встречают синеватый свет и резкий запах озона. Одежда каждого, кто входит в цех, обязательно подвергается стерилизации под действием ультрафиолетовых лучей.
 admin
admin

Большинство лекарств имеет короткие и благозвучные названия. Однако эти названия обычно ничего не говорят нам о химической природе содержащихся в них активных веществ. Если еще раз внимательно осмотреть коробочку с лекарством или прочитать вложенную в нее инструкцию, то иногда можно обнаружить написанное мелким шрифтом точное химическое название препарата.
Среди этих названий часто встречаются настолько сложные и длинные, что нам едва ли удастся их расшифровать или хотя бы выговорить без запинки. Однако именно эти названия точно раскрывают специалисту строение активных веществ. Действительно, лекарственные вещества большей частью имеют очень сложное химическое строение, и их изготовление требует многочисленных трудоемких операций. При этом активная составная часть молекулы нередко имеет очень простое строение, но часто ее приходится присоединять к другим группам. Эти второстепенные группы, на первый взгляд вообще не нужные, так или иначе улучшают лекарственное действие активного фрагмента: например, они могут уменьшить нежелательный побочный эффект лекарства, улучшить его вкус, а главное — способствовать тому, чтобы активный компонент высвобождался только в тех органах тела, где он и должен действовать.
 admin
admin

Чтобы получить представление о лекарственных веществах, синтезируем ангидрометиленлимоннокислый гексаметилентетрамин — препарат, применяемый в качестве антисептика для мочевыводящих путей. Для этого понадобятся 25 мл 35%-ного формалина (Осторожно — яд!), то есть водного раствора метаналя (формальдегида), 10 мл 25 %-ного водного аммиака, 25 г тонко измельченной лимонной кислоты, 10 мл концентрированной соляной кислоты, 100 мл денатурата и 3 г активного угля.
Как показывает сложное название препарата, он образуется в результате соединения двух составных частей — гексаметилентетрамина и ангидрометиленлимонной кислоты. Поэтому вначале нам нужно получить оба эти промежуточных продукта.
В гексаметилентетрамнне шесть метиленовых групп СН2 связаны с четырьмя трехвалентными атомами азота таким образом, что возникает система колец, образующих те-траэдр.
Чтобы его получить, нальем 12,5 мл формалина в маленькую (около 100 мл) колбу Эрленмейера и тщательно охладим ее холодной водой. Постепенно, малыми порциями, добавим 15 мл аммиака. Затем закроем колбу пробкой и оставим ее на 2 часа в холодной воде. После этого прильем еще 2,5 мл аммиака, выдержим в течение 24 часов и выльем раствор в плоскую тарелку или фарфоровую чашку. Тарелку поставим в теплом месте — поблизости от батареи центрального отопления или печи — и выдержим длительное время, чтобы жидкость испарилась.
 admin
admin

Для следующих опытов используем купленную в аптеке салициловую кислоту — кристаллический порошок, трудно растворимый в холодной воде и легко растворяющийся в горячей, а также в спирте и ацетоне.
При осторожном нагревании в пробирке салициловая кислота возгоняется, а при сильном нагревании расщепляется с образованием фенола и диоксида углерода.
Салициловая кислота и многие ее производные дают с солями трехвалентного железа интенсивное фиолетовое окрашивание. Растворим немного салициловой кислоты в воде и добавим несколько капель сильно разбавленного раствора хлорида железа (III). Окраска устойчива при хранении или нагревании раствора. Однако такую окраску с хлоридом железа могут давать и другие органические соединения. Например, растворим в воде кристаллик фенола (Осторожно! Яд!) и смешаем этот раствор с хлоридом железа. При этом тоже появится фиолетовое окрашивание. В двух других пробирочных опытах растворим фенол и салициловую кислоту не в воде, а в спирте.
Теперь окраску с хлоридом железа даст только салициловая кислота.
Возьмем навеску 0,5 г салициловой кислоты, внесем ее в химический стакан и при слабом нагревании растворим в 250 мл воды.
Отберем пипеткой 1 мл раствора и разбавим его в пробирке 9 мл воды. Затем из этой пробирки снова отберем 1 мл и опять в другой пробирке разбавим раствор в 10 раз. В третьей и четвертой пробирке снова разбавим раствор таким же образом. Теперь в каждую из 4 пробирок добавим несколько капель раствора хлорида железа и посмотрим, до какого разбавления можно еще обнаружить фиолетовую окраску.
Салициловая кислота вступает и в некоторые другие реакции, которые могут служить для ее обнаружения и в то же время дают нам наглядное представление о ее химических свойствах.
 admin
admin







 Подготовка к ГИА и ВПР
Подготовка к ГИА и ВПР
