| Темы на форуме | Автор | Дата |
Задача 1. Как в две стадии из уксусного альдегида получить бромэтан?
Решение. Уксусный альдегид можно восстановить водородом до этанола:
t,Ni
СН3СН=О + Н2 → СН3СН2ОН,
а этанол обработать бромоводородной кислотой:
СН3СН2ОН + НBr → СН3СН2Br + Н2О.
Задача 2. Соединение состава С4Н8Сl2 с неразветвленным углеродным скелетом нагрели с водным раствором гидроксида натрия и получили органическое соединение, которое при окислении гидроксидом меди (II) превратилось в соединение состава С4Н8О2. Определите строение исходного соединения.
Решение. Если бы два атома хлора находились у разных атомов углерода, то при обработке щелочью мы получили бы двухатомный спирт, который не окисляется Сu(ОН)2. Если бы два атома хлора находились при одном атоме углерода в середине цепи, то при обработке щелочью мы получили бы кетон, который не окисляется Сu(ОН)2. Следовательно, искомое вещество - 1,1-дихлорбутан, СН3СН2СН2СНСl2. При щелочном гидролизе этого вещества образуется бутановый (масляный) альдегид:
СН3(СН2)2СНСl2 + 2NaOH → СН3(СН2)2СН=О + 2NaCl + Н2O,
который окисляется гидроксидом меди (II) до бутановой (масляной)кислоты:
СН3(СН2)2СН=О + 2Сu(ОН)2 → СН3(СН2)2СООН + Сu2О↓ + 2Н2О.
Ответ. 1,1-дихлорбутан.
Задача 3. Для каталитического гидрирования 17,8 г смеси муравьиного и уксусного альдегидов до соответствующих спиртов потребовалось 11,2 л водорода (н.у.). Определите массовые доли альдегидов в смеси.
Решение. Пусть в смеси находилось х моль НСНО и y моль СН3СНО. тогда масса смеси равна: 30.х+44y = 17,8 г. Для полного гидрирования смеси по уравнениям
НСНО + Н2→СН3ОН,
СН3СНО + Н2→СН3СН2ОН
требуется (х+у) моль водорода, или 11,2/22,4 = 0,5 моль. Решая систему двух уравнений для х и у, находим: х = 0,3, У = 0,2.
Массовые доли альдегидов в смеси равны: w(НСНО) = 0,3-30 / 17,8 = 0,506, или 50,6%, w (СН3СНО) = 0,2-44 / 17,8 = 0,494, или 49,4%.
Ответ. 50,6% муравьиного альдегида, 49,4% уксусного альдегида.
Задача 4. Определите структурную формулу соединения, если известно, что оно состоит из 37,7% С, 6,3% Н и 56,0% Cl (по массе). 6,35 г паров этого соединения занимают объем 1,12 л (н.у.). При гидролизе этого соединения образуется вещество, состоящее из С, Н, О, а при восстановлении последнего образуется вторичный спирт.
Решение. В объеме 1,12 л содержится 1,12/22,4 = 0,05 моль данного вещества. Его молярная масса равна 6,35/0,05 = 127 г/моль. В одном моле вещества содержится 127-0,56 = 71 г Cl (два моль), 127-0,377 = 48 г С (четыре моль) и 127-0,063 = 8 г Н (восемь моль). Формула вещества - С4Н8Сl2.
Вторичные спирты образуются при восстановлении кетонов, следовательно при гидролизе С4Н8Сl2 образуется кетон. Это означает, что два атома хлора находятся при одном атоме углерода в середине цепи. Искомое вещество - 2,2-дихлорбутан, СН3-СН2-ССl2-СН3.
Уравнения реакций:
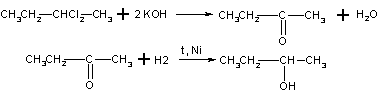
Ответ. 2,2-дихлорбутан, СН3-СН2-ССl2-СН3.
Задача 5. К 1,17 г смеси прогтанола-1 и неизвестного альдегида добавили аммиачный раствор 5,80 г оксида серебра и слегка нагрели. Выпавший при этом осадок отфильтровали, а непрореагировавший оксид серебра перевели в хлорид серебра, масса которого оказалась равной 2,87 г. Определите строение взятого альдегида, если молярное отношение альдегида к спирту в исходной смеси равно 3:1.
Решение. С оксидом серебра в аммиачном растворе реагирует только альдегид:
NН3
RCH=O + Ag2O- → RCOOH + 2Ag↓
Непрореагировавший Ag2O перевели в AgCl действием избытка соляной кислоты:
Ag2O + 2HCl = 2АgСl + Н2О.
v(AgCl) = 2,87/143,5 = 0,02 моль. В эту реакцию вступило 0.02/2 = 0,01 моль Аg2О, а всего было 5,8/232 = 0,025 моль Аg2О; следовательно, в реакцию с альдегидом вступило 0,025-0,01 = 0,015 моль Ag2O. v(RCH=O) = v(Ag2O) = 0,015 моль.
Пропанола-1 в смеси было в 3 раза меньше, чем альдегида: v(CH3CH2CH2OH) = 0,015/3 = 0,005 моль. Масса пропанола-1 равна 0,005*60 = 0,3 г, а общая масса смеси - 1,17 г, следовательно масса альдегида равна 1,17-0,3=0,87 г. Молярная масса альдегида: M(RCH=O) = 0,87/0.015 = 58 г/моль, что соответствует уксусному альдегиду СН3-СН=О.
Ответ. Уксусный альдегид, СН3-СН=О.
Своё Спасибо, еще не выражали..
 admin
admin







 Подготовка к ГИА и ВПР
Подготовка к ГИА и ВПР
