| Темы на форуме | Автор | Дата |
Химической связи. Ковалентная связь
Понятие химической связи
Образование молекул из атомов приводит к выигрышу энергии, так как в обычных условиях молекулярное состояние устойчивее, чем атомное. Учение о строении атомов объясняет механизм образования молекул, а также природу химической связи.
У атома на внешнем энергетическом уровне может содержаться от одного до восьми электронов. Если число электронов на внешнем уровне атома максимальное, которое он может вместить, то такой уровень называется завершенным. Завершенные уровни характеризуются большой прочностью. Таковы внешние уровни атомов благородных газов: у гелия на внешнем уровне два электрона (s2), у остальных - по восемь электронов (ns2np6). Внешние уровни атомов других элементов незавершенные и в процессе химического взаимодействия они завершаются.
Химическая связь образуется за счет валентных электронов, но осуществляется она по-разному. Различают три основных типа химических связей: ковалентную, ионную и металлическую.
Ковалентная связь
Механизм возникновения ковалентной связи рассмотрим на примере образования молекулы водорода:
Н + Н = Н2; ∆H
= - 436 кДж/мольЯдро свободного атома водорода окружено сферически симметричным электронным облаком, образованным 1 s-электроном. При сближении атомов до определенного расстояния происходит частичное перекрывание их электронных облаков (орбиталей) 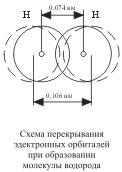 . В результате между центрами обоих ядер возникает молекулярное двухэлектронное облако, обладающее максимальной электронной плотностью в пространстве между ядрами; увеличение же плотности отрицательного заряда благоприятствует сильному возрастанию сил притяжения между ядрами и молекулярным облаком.
. В результате между центрами обоих ядер возникает молекулярное двухэлектронное облако, обладающее максимальной электронной плотностью в пространстве между ядрами; увеличение же плотности отрицательного заряда благоприятствует сильному возрастанию сил притяжения между ядрами и молекулярным облаком.
Итак, ковалентная связь образуется в результате перекрывания электронных облаков атомов, сопровождающегося выделением энергии. Если у сблизившихся до касания атомов водорода расстояние между ядрами составляет 0,106 нм, то после перекрывания электронных облаков (образования молекулы Н2) это расстояние составляет 0,074 нм . Обычно наибольшее перекрывание электронных облаков осуществляется вдоль линии, соединяющей ядра двух атомов. Химическая связь тем прочнее, чем больше перекрывание электронных орбиталей. В результате возникновения химической связи между двумя атомами водорода каждый из них достигает электронной конфигурации атома благородного газа гелия.
Изображать химические связи принято по-разному:
1) с помощью электронов в виде точек, поставленных у химического знака элемента. Тогда образование молекулы водорода можно показать схемой
H∙ + H∙ →H:H
2) с помощью квантовых ячеек (орбиталей), как размещение двух электронов с противоположными спинами в одной молекулярной квантовой ячейке:
1s1 1s1
↑ ↓
\ / или ↑ + ↓ → ↑↓
1s2
↑↓
Схема, расположенная слева, показывает, что молекулярный энергетический уровень ниже исходных атомных уровней, а значит, молекулярное состояние вещества более устойчиво, чем атомное;
3) часто, особенно в органической химии, ковалентную связь изображают черточкой (штрихом) (например, Н—Н), которая символизирует пару электронов.
Ковалентная связь в молекуле хлора также осуществляется с помощью двух общих электронов, или электронной пары:
Неподеленная Неподеленная
пара электронов, → ![]() ← пара электронов,
← пара электронов,
в атоме их 3 ↑ ↑ в молекуле их 6.
неспаренный общая или
электрон поделенная
пара электронов
Как видно, каждый атом хлора имеет три неподеленные пары и один неспаренный электрон. Образование химической связи происходит за счет неспаренных электронов каждого атома. Неспаренные электроны связываются в общую пару электронов, называемую также поделенной парой.
Если между атомами возникла одна ковалентняя связь (одна общая электронная пара), то она называется одинарной; если больше, то кратной двойной (две общие электронные пары), тройной (три общие электронные пары).
Одинарная связь изображается одной черточкой (штрихом), двойная - двумя, тройная - тремя. Черточка между двумя атомами показывает, что у них пара электронов обобщена, в результате чего и образовалась химическая связь. С помощью таких черточек изображают структурные формулы молекул.
Итак, в молекуле хлора каждый его атом имеет завершенный внешний уровень из восьми электронов (s2p6), причем два из них (электронная пара) в одинаковой мере принадлежат обоим атомам. Перекрывание электронных орбиталей при образовании молекулы показано на рис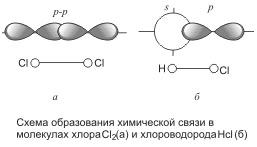
Несколько по-иному изображают связь в молекуле кислорода О2. Экспериментально установлено, что кислород является парамагнитным веществом (втягивается в магнитное поле). В его молекуле имеется два неспаренных электрона. Структуру этой молекулы можно изобразить так:
:О:О: или :О—О:
Одназначное решение об изображении электронной структуры молекулы кислорода еще не найдено. Однако ее нельзя изображать так:
:О::О: или О=O
В молекуле азота N2 атомы имеют три общие электронные пары:
:N: + :N: → :N::N:
Очевидно, молекула азота прочнее молекулы кислорода или хлора, чем и обусловлена значительная инертность азота в химических реакциях.
Химическая связь, осуществляемая электронными парами, называется ковалентной. Это двухэлектронная и двухцентровая (удерживает два ядра) связь. Соединения с ковалентной связью называются гомеополярными или атомными
Разновидности ковалентной связи. Механизм образования
Различают две разновидности ковалентной связи: неполярную и полярную.
В случае неполярной ковалентной связи электронное облако, образованное общей парой электронов, или электронное облако связи, распределяется в пространстве симметрично относительно ядер обоих атомов. Примером являются двухатомные молекулы, состоящие из атомов одного элемента: Н2, Сl2, О2, N2, F2 и др., в которых электронная пара в одинаковой мере принадлежит обоим атомам.
В случае полярной ковалентной связи электронное облако связи смещено к атому с большей относительной электроотрицательностью. Примером могут служить молекулы летучих неорганических соединений: НСl, Н2О, Н2S, NН3 и др.
Образование молекулы НСl можно представить схемой
Н.+ .Сl: = Н :Cl:
Электронная пара смещена к атому хлора, так как относительная электроотрицательность атома хлора (2,83) больше, чем атома водорода (2,1).
Ковалентная связь образуется не только за счет перекрывания одноэлектронных облаков, - это обменный механизм образования ковалентной связи.
Возможен и другой механизм ее образования - донорно-акцепторный. В этом случае химическая связь возникает за счет двухэлектронного облака одного атома и свободной орбитали другого атома. Рассмотрим в качестве примера механизм образования иона аммония 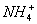 .
.
В молекуле аммиака атом азота имеет неподеленную пару электронов двухэлектронное облако):
 . . |
У иона водорода свободна (не заполнена) 1s-орбиталь, что можно обозначить как □H
+. При образовании иона аммония двухэлектронное облако азота становится общим для атомов азота и водорода, т.е. оно превращается в молекулярное электронное облако. А значит, возникает четвертая ковалентная связь. Процесс образования иона аммония можно представить схемой<>  |
+ □H+ → |  |
Заряд иона водорода становится общим (он делокализован, т.е. рассредоточен между всеми атомами), а двухэлектронное облако (неподеленная электронная пара), принадлежащее азоту, становится общим с водородом. В схемах изображение ячейки □ часто опускается.
Атом, предоставляющий неподеленную электронную пару, называется донором, а атом, принимающий ее (т.е. предоставляющий свободную орбиталь), называется акцептором.
Механизм образования ковалентной связи за счет двухэлектронного облака одного атома (донора) и свободной орбитали другого атома (акцептора) называется донорно-акцепторным. Образованная таким путем ковалентная связь называется донорно-акцепторной или координационной связью.
Однако это не особый вид связи, а лишь иной механизм (способ) образования ковалентной связи. По свойствам четвертая N—Н-связь в ионе аммония ничем не отличается от остальных трех.






 Подготовка к ГИА и ВПР
Подготовка к ГИА и ВПР
