Примеры решения задач 2
18-02-2010, 18:14. Разместил: admin
Задача 1. С помощью каких химических реакций можно очистить пропан от примеси пропена?
Решение. Пропен можно поглотить бромной водой:
СН3-СН=СН2 + Вr2 → СН3-СНВr-СН2Вr
или водным раствором перманганата калия:
СН3-СН=СН2 + [О] + Н2О → СН3-СН(ОН)-СН2ОН.
Пропан с этими веществами не реагирует и улетучивается.
Задача 2. Этиленовый углеводород массой 7,0 г присоединяет 2,24 л (н.у.) бромоводорода. Определите молярную массу и строение этого углеводорода, если известно, что он является цис-изомером.
Решение. Этиленовые углеводороды присоединяют бромоводород по уравнению:
CnH2n + HBr → CnH2n+1Br.
v(HBr) = 2,24/22,4 = 0,1 моль. v(CnH2n) = v(HBr) = 0,1 моль. M(CnH2n) = 7,0/0,1 = 70 г/моль, следовательно, n = 5. Существует 5 структурных изомеров этиленовых углеводородов состава С5Н10:
СН3-СН2-СН2-СН=СН2 СН3-СН2-СН=СН-СН3
пентен-1 пентен-2
![]()
2-метилбутен-1 2-метнлбутен-2 З-метилбутен-1
Из этих веществ только пентен-2 имеет цис-транс-нзомеры:
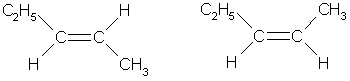
транс-пентен-2 цис-пентен-2
Ответ. Цис-пентен-2.
Задача 3. Сколько существует индивидуальных веществ состава С3Н5Сl. обесцвечивающих бромную воду? Приведите структурные формулы молекул этих веществ.
Решение. С3Н5Сl - это монохлорпроизводное от углеводорода С3Н6. Это вещество обесцвечивает бромную воду, следовательно, имеет в своем составе двойную связь. Три атома углерода могут образовать только неразветвленный углеродный скелет с концевой двойной связью:
С-С = С.
Структурная изомерия возможна только за счет положения атома хлора относительно двойной связи:
СН3-СН = СНСl СН3-ССl = СН2 Сl-СН2-СН = СН2
1-хлорпропен 2-хлорпропен 3-хлорпропен
1-хлорпропен может существовать в виде цис-транс-изомеров:
транс-1 –хлорпропен цис -1-хлорпропен
Ответ. 4 изомера.
Задача 4. При взаимодействии 11,2 л (н.у.) смеси изомерных углеводородов, представляющих собой газы с плотностью по водороду 21, с бромной водой получено 40,4 г соответствующего дибромпроизводного. Определите строение этих углеводородов и содержание каждого из них в смеси (в % по объему).
Решение. Молярная масса изомерных углеводородов равна: M(СхНу) = 21*2 = 42 г/моль, следовательно, углеводороды имеют формулу С3Н6. Такую молекулярную формулу имеют два вещества - пропен и циклопропан. Пропен реагирует с бромной водой:
СН3 - СН = СН2 + Вr2 → СН3 – СНВr - СН2Вr.
Молярная масса дибром производного равна: М(С3Н6Вr2) = 202 г/моль, а его количество: v(C3H6Br2) = 40,4/202 = 0,2 моль. Следовательно, в исходной смеси было 0,2 моль пропена. Общее количество углеводородов в смеси было равно 11,2/22,4 = 0,5 моль; оставшиеся 0,3 моль приходятся на долю циклопропана, который не взаимодействует с бромной водой.
Объемные доли газов в смеси равны их мольным долям: j( пропена) = 0,2/0,5 = 0,4, или 40%, j (циклопропана) = 0,6, или 60%,
Ответ. 40% пропена, 60% циклопропана.
Задача 5. При пропускании алкена через избыток раствора перманганата калия масса выпавшего осадка оказалась в 2,07 раза больше массы алкена. Установите формулу алкена.
Решение. Алкены окисляются водным раствором перманганата калия по общему уравнению:
ЗСnН2n + 2KМnO4 + 4Н2O = 3CnH2n(OH)2 + 2MnO2↓ + 2KOH
.Из 3 моль алкена (массой 3-(12n+2n) = 42n) образуется 2 моль МnО2 (массой 2*87 = 174 г). По условию задачи
42n –2,07= 174,
откуда n = 2. Искомый алкен — этилен. С2Н4.
Ответ. С2Н4.
Вернуться назад